En aquesta pàgina es proposen protocols de procediments experimentals per a obtenir els valors de diferents magnituds i/o constants fonamentals de la Física i la Química que es poden portar a terme en un laboratori escolar o fins i tot a cassa dels estudiants.
L’idea no és aconseguir resultats homologables per a les constants, malgrat que en molts casos s’aproximaran prou, si més no l’obtenir valors de l’ordre de magnitud i discutir les procediments i resultats amb l’alumnat.
Mesura de la velocitat de la llum

La mesura de la velocitat de la llum per mètodes ortodoxes no està a l’abast d’un laboratori escolar, sinó és a partir de trobar els valors de la permeabilitat (μ0) i la permitivitat (ε0) del buit i després calcular la velocitat de la llum (c):
μ0·ε0·c2 = 1
Malgrat aixó, Benjamín Montesinos ens explica com mesurar la velocitat de la llum amb un microones i regalèssia. Aquest experiment i d’altres amb un forn de microones també es troba en l’article Microones en un forn, de Lorenzo Ramírez, en el número 4 (2006) de la revista Ciències. Més acurat és el procediment, també amb un microones, que proposen Alejandro del Mazo i Santiago Velasco (2022) a l’article Determinación de la longitud de onda de las microondas de un horno a través de sus fugas de radiación en la revista Eureka sobre Enseñanza y Divulgación de las Ciencias.
Permitivitat elèctrica

A l’entrada Determinar experimentalment amb Arduino la permitivitat elèctrica de l’aire es descriu com obtenir el valor de la permitivitat elèctrica a l’aire (ε0) amb un condensador pla paral·lel fet artesanalment i amb un dispositiu Arduino.
Permeabilitat magnètica

A l’entrada Determinació experimental de la permeabilitat magnètica amb telèfon es descriu com obtenir el valor de la permeabilitat magnètica a l’aire (µ0) amb el sensor magnètic d’un telèfon mòbil i una bobina construïda artesanalment.
Determinació de la contant de Planck

A l’entrada Determinació de la constant de Planck en un laboratori escolar realitzada amb motiu de l’Any Internacional de la Ciència i la Tecnologia Quàntica 2025 (IYQ2025) es descriu com obtenir la constant de Planck a partir de l’electroluminescència de díodes de diferents colors i es discuteixen diferents variants.
Càlcul de la contant de Rydberg
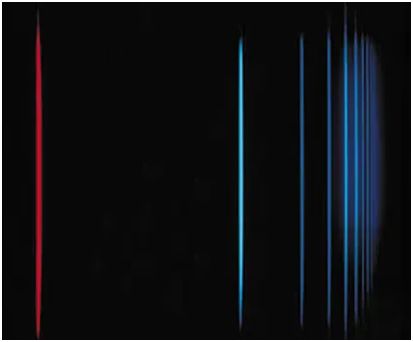
A l’entrada L’espectre de l’hidrogen i la constant de Rydberg realitzada amb motiu de l’Any Internacional de la Ciència i la Tecnologia Quàntica 2025 (IYQ2025) es descriu com obtenir la constant de Rydberg a partir de les línies espectrals de l’hidrogen. Aquesta entrada està elaborada a partir d’una idea de la Guía del laboratorio de física (1969) del Physical Science Study Committee (PSSC).
A diferència de la majoria dels treballs al respecte que he vist publicats (també el del PSSC) i que utilitzen un espectre-goniòmetre per a mesurar les longituds d’ona de les línies, aquí proposo usar un espectroscopi de mà quantitatiu que indiqui directament el seu valor, de manera que l’alumnat no tingui la dificultat més gran en la manipulació d’un aparell. Espectroscopis d’aquesta mena que tinguin un error de mesura de ± 5 nm es poden comprar a preus assequibles, però també construir amb cartolina.
Decaïment radioactiu

Protocol per realitzar una simulació del decaïment d’una mostra radioactiva i el càlcul del període de semidesintegració a partir del llançament de daus o monedes.
Mesura de la velocitat del so

Recopilatori de diferents propostes per mesurar la velocitat del so. N’hi ha des del mètode més tradicional d’utilitzar la ressonància en un tub parcialment submergit en aigua fins a la mesura directa del temps que triga un so en desplaçar-se una distancia.
L’acceleració de la gravetat

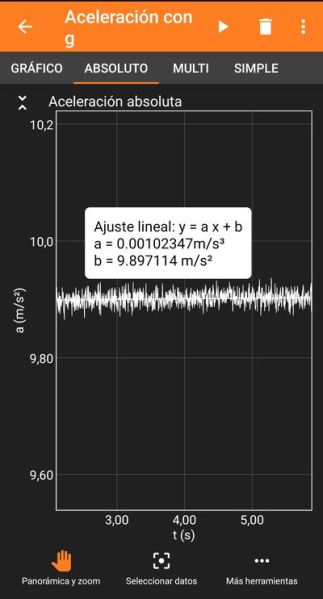
Avui en dia per a conèixer el valor de l’acceleració de la gravetat en el lloc on un mateix es troba no hi ha més que ficar en marxa al telèfon mòbil una aplicació que mesuri aquest valor, com per exemple Phyphox a l’apartat Aceleración con g, i fer la mesura mantenint el telèfon immòbil. El resultat el tenim en la captura de pantalla del costat.
Si volem introduir una mica més de física podem realitzar qualsevol dels experiments que mesurin directa o indirectament el temps que triga en caure lliurement un objecte.
- En Cálculo de la aceleración en la caída libre es mesura amb un telèfon el temps que tarda en caure al terra una bola.
- Es pot deixar caure el mateix telèfon com en L’acceleròmetre i la caiguda lliure.
- En els protocols del CDEC Moviment de caiguda d’un regle (per l’alumnat i el professorat) s’explica com estudiar amb un datalogger la caiguda lliure de una tanca, el que també es por fer amb un telèfon i una fotoresistència com en Estudi de moviments amb fotocèl•lula.
I sense voler ser exhaustius, estudiant el moviment d’un pèndol simple també es pot obtenir fàcilment el valor de g. El període del pèndol es pot mesurar de moltes diverses maneres:
- Amb un cronòmetre de rellotge o de mòbil, com fa en un primer experiment l’alumnat de Secundaria a l’IES “Leonardo Da Vinci” d’Alacant en Péndulo simple I. Planteamiento, hipótesis y diseños experimentales.
- Amb els fotogrames d’una gravació de vídeo del moviment i VCL, per exemple, i encara més sofisticat amb el punteig de les imatges amb Tracker, com a l’Estudio del péndulo simple con tracker.
- Amb l’acceleròmetre o el sensor de proximitat d’un telèfon com per exemple a Oscilaciones del péndulo medidas con el sensor de proximidad.
- Etc., etc.
Caminant amb Eratóstenes. Mesura del radi de la Terra
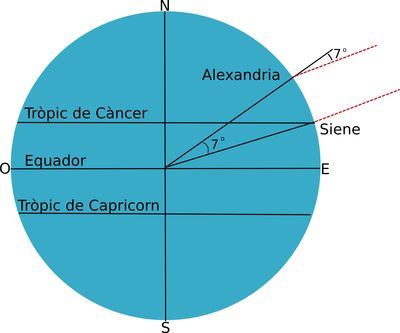
Protocol per la mesura del radi de la Terra a qualsevol hora del dia, del mes de juny, setembre o octubre.
Resultats de la mesura del radi de la Terra realitzada per l’alumnat de 4t d’ESO de l’IES Maria Rúbies de Lleida en 2005, l’Any Mundial de la Física.
La mesura de l’ombra del Sol, per l’Associació Astronòmica de Barcelona, ASTER.
Determinació del zero absolut de temperatures

Hi ha diverses maneres d’estudiar la relació entre les magnituds involucrades en l’equació dels gasos ideals i que permeten obtenir per extrapolació el valor del zero absolut de temperatura. A l’any 2021 vaig fer un recopilatori sobre les lleis dels gasos, i com es veu en els experiments relacionats amb aquestes lleis es poden obtenir valors prou bons que oscil·len entre -274 i -280 ºC.
Llei de Charles i Gay-Lussac
Segona llei de Gay-Lussac: Pressió temperatura
- Amb matràs al bany Maria
- Pressió temperatura amb termòmetre digital i telèfon amb baròmetre en un pot de vidre
- Pressió temperatura amb sensor de P, T i H amb arduino (per bluetooth) en un pot de vidre
Determinació de la constant universal dels gasos

Per a calcular R, la constant que relaciona les magnituds a l’equació dels gasos ideals també podem acudir a algun altre dels experiments llistats al recopilatori sobre les lleis dels gasos que ja he comentat a dalt, els que relacionen la pressió i el volum.
En tot cas s’ha de trobar la massa de gas o el nombre de mols amb que es fa l’experiment com proposen en el protocol La constant universal dels gasos, del material de suport pel batxillerat internacional (2007), a partir del valor de la pressió atmosfèrica on es fa l’experiment.
Una alternativa molt xula és la de Antonio Tomás Serrano i Jerónimo Hurtado-Pérez (2020), Determinación de la constante de los gases usando un manómetro y una balanza, en el volum 17, n 3 de la Revista Eureka sobre Enseñanza y Divulgación de las Ciencias.
Determinació del nombre d’Avogadro

Encara que el que fan els científics per a obtenir un valor per al nombre d’Avogadro sigui comptar el nombre d’àtoms en una esfera de silici-28 d’alta puresa, aquí us proposo dos mètodes que tradicionalment s’han portat a terme als laboratoris escolars: el de la tac d’oli i el de l’electròlisi.
Com es pot calcular la constant d’Avogadro?. Protocol del CDEC que utilitza la mesura del volum de l’àcid oleic.
Determinación de la constante de Avogadro mediante un experimento de electrólisis realizado con productos de bajo coste, de Tomás-Serrano i Rafael Garcia-Molina, publicat en el núm 113 (2017) de la Revista Anales de Química.
Determinació de la constant de Faraday (i la càrrega de l’electró)

La constat de Faraday (F) forma part de l’equació que regeix l’electròlisi de qualsevol ió tal que la massa de l’element que es diposita en un elèctrode és:
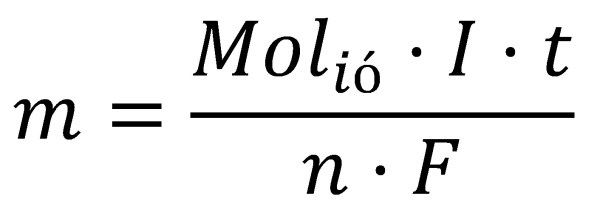
On m és la massa dipositada, Molió és la massa molar de l’ió, I la intensitat de corrent, t el temps que circula el corrent, n la càrrega de l’ió i F la constant de Faraday.
Un bon sistema per obtenir del valor de la constat de Faraday, per tant, es fer-lo mitjançant una electròlisi. El professor Salvador Gil ens proposa fer-lo amb el Sulfat de coure en el Proyecto 86 Estimación de la carga del electrón (pag 344) del capítulo 29 en la part 3 del llibre Experimentos de Física de bajo costo usando TICs.
Amb un aparell d’electròlisi (voltàmetre de Hofmann) també es pot determinar la constant de Faraday mitjançant l’electròlisi de l’aigua.
Una vegada aconseguida la constant de Faraday (F) es pot determinar la càrrega de l’electró si es coneix el nombre d’Avogadro (NA) ja que estan relacionats per:
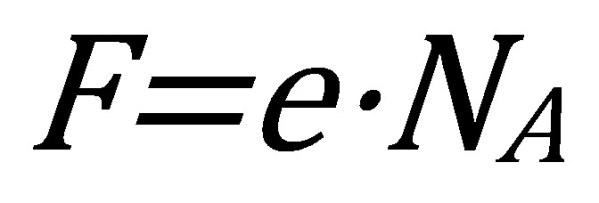
Encara que tradicionalment s’ha fet al revés, és a dir, aconseguir el valor del nombre d’Avogadro a partir del valor de la càrrega de l’electró amb l’electròlisi d’una sal de plata, de forma anàloga a com hem vist que feien a dalt Antonio Tomás-Serrano i Rafael Garcia-Molina.
[…] Determinació experimental de magnituds i constants físicoquímiques fonamentals (o no tant) […]
[…] Determinació experimental de magnituds i constants físicoquímiques fonamentals (o no tant) […]